М т отсутствует что это значит?
Тело без антитела: почему вам вообще не нужны антитела к коронавирусу
Есть целая группа людей, у которых нет антител к коронавирусу, но есть иммунитет. Или же человек переболел, антитела появились, но потом пропали, а иммунитет остался. Долгое время не было тестов, которые бы позволили выявить имеющийся иммунитет. Теперь они появились. Мы поговорили с Дмитрием Потеряевым, заместителем генерального директора по науке «МБЦ Генериум», в стенах которого был изобретён такой тест.
 Дмитрий Потеряев
Дмитрий Потеряев
— Известно множество случаев, когда у выздоровевших пациентов отсутствовали антитела к коронавирусу. Как им удалось победить болезнь?
— Защитная реакция организма против любых инфекций, в том числе против COVID-19, не сводится к одним лишь антителам. Есть еще и Т-клеточный ответ. Он связан не с антителами, а с мощными клетками-убийцами, или Т-лимфоцитами, которые активируются, когда в организм попадает вирус. Какая-то часть этих «убийц» остается в виде клеток памяти. Они-то в дальнейшем и «узнают» перенесенный вирус.
Если у выздоровевшего уровень антител низкий, то побороть болезнь он мог либо с помощью врожденного иммунитета, либо с помощью Т-клеточного ответа. Отсутствие последнего встречается гораздо реже, чем отсутствие антител в крови.
— Если антитела могут исчезнуть за пару месяцев, то как долго сохраняется Т-клеточный ответ?
— По поводу текущего коронавируса мы знаем, что не менее 6 месяцев. Что касается его ближайших родственников, например, коронавирусов, вызывающих SARS и MERS, необходимый уровень Т-клеток поддерживается уже более 10 лет. Это показали данные наблюдений за выздоровевшими пациентами.
Насколько Т-клеточный иммунитет способен реально защитить человека от COVID-19, пока сложно сказать. По имеющейся информации можно сделать вывод, что защитная функция, вероятно, сохраняется годами.
— На чем основана ваша технология выявления Т-клеток к коронавирусу?
— В лаборатории активность Т-клеток в ответ на узнавание возбудителя измеряют при помощи технологии ELISPOT. Суть метода заключается в следующем: из свежей венозной крови выделяются Т-лимфоциты, среди которых могут быть те, кто имеет специфические рецепторы к белкам, антигенам коронавируса. Т-лимфоциты стимулируются путем добавления в специальную среду белков-антигенов коронавируса. Если контакт организма с вирусом был, рецептор Т-клетки свяжется с белками коронавируса, Т-лимфоцит активируется, и мы это увидим.
Исследование, которое проводили в июне среди почти 3 тыс. британских медиков, полиции и пожарных, показало, что при отсутствии антител, определенный уровень специфических к коронавирусу Т-клеток может защищать от инфекции. У испытуемых проводили анализ на Т-клеточный иммунитет методом ELISPOT, а также определяли антитела. Потом за участниками наблюдали в течение 4 месяцев. Среди тех, кто имел антитела к коронавирусу, не заболел никто. Но что интереснее, около 300 человек, не имевших антител, обладали высоким уровнем Т-клеточного ответа. В этой группе также никто не заболел.
Исследователи также отметили важность того факта, что ни один человек с высоким уровнем Т-клеток не смог заразится COVID-19 в течение следующих четырех месяцев.
— Сейчас популяционный иммунитет к COVID-19 оценивают по данным тестов на антитела. Но если для иммунитета наличие антител необязательно, означает ли это, что в действительности защищена большая часть населения?
— Антитела — полезный инструмент для оценки иммунитета. Но, конечно, мы недооцениваем уровень защищенности населения, ту его часть, которая обладает Т-клеточным иммунитетом, если опираемся только на серологические (антительные) тесты.
— Как вы планируете внедрять методику в реальную медицинскую практику? Возможно ли проведение массового тестирования населения на Т-клеточный иммунитет?
— Сейчас мы хотим понять, насколько наши тесты будут востребованы в практике, насколько врачи и органы здравоохранения заинтересуются в проведении массового тестирования. Пока такие тесты проводят в одной частной клинике.
Ведущие программы «Жить здорово!» побывали в лаборатории, где среди первых прошли тест на Т-клетки
А исследовательской группе ученых из Кембриджского университета, с помощью современных микроскопов, удалось снять работу клеток иммунитета Т-киллеров в высоком разрешении. На видео показана работа этих клеток вживую.
Т-киллеры — это белые кровяные тельца, специализирующиеся на поражении вирусов и опухолевых клеток. В одной чайной ложке крови их около пяти миллионов. Т-киллеры, перемещаясь по организму, уничтожают клетки, инфицированные вирусами или бактериям.
Клетки иммунной системы защищают организм от патогенных микроорганизмов. Если клетки в организме человека заражены вирусами, то клетки Т-киллеры иммунной системы выявляют и уничтожают пораженные клетки.
Анти-HER2 терапия в лечении рака молочной железы

Анти-HER2 терапия в лечении рака молочной железы
Процессы роста и размножения всех клеток в организме находятся под жестким регулирующим контролем генов, которые способных запускать или останавливать их. В норме в организме поддерживается баланс между появлением новых клеток и гибелью старых. В опухолевых клетках процессы размножения клеток выходят из под контроля. Зачастую это происходит по причине возникновения «сбоев» в работе определенных генов, играющих наиболее важную роль в контроле над делением клеток.
HER2 (аббревиатура от английского human epidermal growth factor receptor 2 – рецептор фактора роста эпидермиса) является одним из таких генов. Этот ген может также обозначаться как «HER2-neu» или «ERBB2», эти названия являются синонимами. Его неправильная работа обнаруживается во многих случаях развития рака молочной железы и приводит к активной выработке в клетках одноименного белка (HER2), что заставляет клетки быстро делиться. Когда в клетке образуется избыточное количество белка HER2, говорят об амплификации этого гена. Амплификация HER2 обнаруживается примерно у 25% пациенток с диагнозом рака молочной железы. Её наличие приводит к повышению агрессивности опухолевых клеток. Вследствие высокой важности знания HER2-статуса опухоли, определение наличия амплификации HER2 является или избыточной выработки белка HER2 является одним из стандартных методов обследования, и проводится у всех пациенток с диагнозом рака молочной железы. Кроме того, в ряде исследований была продемонстрирована клиническая значимость выработки HER2 при раке желудка, по этой причине препараты, подавляющие активность этого белка также применяются для лечения рака желудка.
В чем особенности HER2-положительного рака молочной железы?
Изначально HER2-позитивный рак молочной железы был одним из наиболее агрессивных разновидностей этого заболевания, который характеризовался очень быстрым темпом роста опухоли, высоким риском развития рецидива болезни и появления отдаленных метастазов. Тем не менее, в настоящее время разработано множество препаратов, подавляющих активность этого белка (см. ниже). Они продемонстрировали высокую эффективность в лечении HER2-положительного рака молочной железы, превратив этот подтип рака в один из относительно благоприятных вариантов заболевания. Проведение целенаправленной («таргетной») терапии, блокирующей активность HER2, позволяет значительно повысить эффективность лечения и резко снизить риск развития рецидива рака молочной железы или добиться длительного контроля над болезнью в случае лечения её поздних стадий.
Кому назначаются препараты, блокирующие активность HER2?
Необходимо отметить, что применение препаратов, блокирующих активность HER2, целесообразно только в том случае, если в опухоли есть повышенная выработка этого белка вследствие наличия амплификации гена HER2. Если она отсутствует, раковые клетки не вырабатывают этот белок, следовательно, назначение препаратов, блокирующих активность этого белка не приведет к желаемому результату. По этой причине перед началом лечения всем пациенткам с диагнозом рака молочной железы перед началом лечения проводится специальное обследование, направленное на определение повышенной выработки HER2. Эта информация критически важна для правильного лечения рака молочной железы.
Как определяется HER2 статус опухоли?
В процессе диагностики рака молочной железы небольшой кусочек опухолевой ткани путем биопсии забирается для проведения иммуногистохимического исследования. Как правило, одновременно проводится определение наличия экспрессии (выработки) опухолевыми клетками рецепторов женских половых гормонов, HER2-статуса опухолевых клеток, а также темпов её роста (индекс Ki-67). При проведении этого исследования на опухолевые клетки наносятся специальные «красители», которые окрашивают HER2 в случаях, когда он содержится в клетках в большом количестве. Иммуногистохимическое исследование оценивает наличие гиперпродукции белка HER2 опухолевыми клетками.
По результатам иммуногистохимического определения HER2 статуса опухоли может быть получен один из следующих результатов:
0 баллов – в опухоли не отмечено признаков экспрессии HER2 (результат исследования отрицательный, назначение анти-HER2 препаратов нецелесообразно);
1+ — в опухолевых клетках обнаружена незначительная экспрессия HER2 (результат исследования отрицательный);
2+ — в опухолевых клетках обнаружена умеренная экспрессия HER2 (результат сомнительный, требуется проведение дополнительного исследования, см. ниже);
3+ — в опухолевых клетках обнаружена повышенная экспрессия HER2 (результат положительный, назначение анти-HER2 препаратов целесообразно).
Если по результатам иммуногистохимического исследования была выявлена выраженная экспрессия HER2 (3+), пациентке показано назначение препаратов, блокирующих активность этого белка, так как опухолевые клетки активно вырабатывают этот белок и процессы их роста зависят от его функционирования. Если результат исследования отрицательный (0 или 1+) назначение такого лечения не приведет к желаемому результату.
Получение сомнительного результата (2+) означает, что по результатам иммуногистохимического исследования достоверно определить наличие экспрессии HER2 не удалось и необходимо проведение дополнительных методов исследования, например, т.н. «флюоресцентной гибридизации in situ» (FISH) или схожего с ней метода CISH. Эти методы позволяют напрямую оценить наличие амплификации HER2. По результатам проведения этих тестов может быть получен положительный или отрицательный ответ. Положительный ответ означает, что была выявлена амплификации HER2 и целесообразно назначение анти-HER2 терапии.
Какие существуют лекарственные препараты для лечения HER2-позитивного рака молочной железы?
На данный момент разработано и внедрено в клиническую практику 4 препарата, подавляющих активность HER2. Они несколько различаются по структуре и механизму действия, а также по показаниям к применению, эти лекарства могут назначаться как в комбинации с другими препаратами, например химиотерапевтическими агентами, так и самостоятельно (в монотерапии). В этом разделе представлено краткое описание этих препаратов.
Трастузумаб – лекарственный препарат, который представляет собой белок (моноклональное антитело), сконструированный таким образом, чтобы избирательно связываться с HER2 и «закрывать» его, не давая ему возможности нормально функционировать и провоцировать процессы роста и деления опухолевых клеток. Трастузумаб является препаратом, который наиболее часто назначается пациенткам с HER2-положительным раком молочной железы. Он применяется в сочетании с химиотерапией в качестве пред- или послеоперационной терапии данного заболевания, а также для первоначального лечения поздних его поздних стадий. Препарат выпускается как в виде раствора для внутривенных капельных введений, так и в виде раствора для подкожных введений. Трастузумаб-эмтанзин (T-DM1) – комбинированный препарат, который содержит молекулы трастузумаба, соединенные с противоопухолевым препаратом эмтанзином, который оказывает губительное действие на клетки. Препарат сконструирован таким образом, что молекулы трастузумаба связываются со своей мишенью на поверхности опухолевых клеток, после чего эмтанзин проникает в них и вызывает гибель раковых клеток. Помимо лечения рака молочной железы трастузумаб также применяется для лечения рака желудка в случае выявления в опухоли гиперэкспрессии HER2. Препарат вводится внутривенно капельно.
Пертузумаб – также как и трастузумаб, пертузумаб представляет собой моноклональное антитело к HER2, однако в отличие от трастузумаба он связывается с другим участком этого белка. Препарат назначается в комбинации с трастузумабом и позволяет повысить эффективность лечения. Препарат вводится внутривенно капельно.
Лапатиниб – препарат, блокирующий сигнальный путь, который проводит сигналы от HER2. Препарат применяется для лечения пациенток, у которых было отмечено прогрессирование на фоне применения режимов лечения с использованием трастузумаба, а также для лечения HER2-положительного гормонозависимого рака молочной железы, в этом случае лапатиниб применяется в комбинации с гормонотерапией. Препарат выпускается в виде таблеток и принимается внутрь.
Указанные препараты назначаются только пациенткам с HER2-положительными опухолями (экспрессия HER2 3+ при проведении иммуногистохимического исследования или выявленная амплификация гена при проведении FISH или схожего метода исследования).
Может ли HER2 статус изменяться в процессе проведения лечения?
Необходимо отметить, что HER2 статус опухоли может меняться в процессе проведения лечения как результат изменений, происходящих в раковых клетках. Клетки опухоли ищут способ выжить на фоне проводимой терапии и постоянно изменяются. Например, в случае, если произошел рецидив исходно HER2-положительной опухоли, во вновь выявленных опухолевых очагах может отмечаться исчезновение выработки этого белка и утрата зависимости опухолевых клеток от влияния этого гена. Возможно и обратное – появление гиперэкспрессии HER2 в опухолях, которые исходно не вырабатывали этот белок. По этой причине в случае развития рецидивов или появления метастазов врач может рекомендовать повторное проведение биопсии и проведение нового тестирования для определения HER2 статуса опухоли.
Расшифровка МРТ головного мозга
Результаты МРТ головного мозга – это серия снимков в нескольких плоскостях, представляющих собой послойные виртуальные срезы толщиной в пару миллиметров, сделанные через исследуемую область. Полная и точная интерпретация снимков магнитно-резонансной томографии – работа врача-рентгенолога, имеющего специализацию в соответствующей области. Задача данного материала – знакомство с основными принципами расшифровки результатов МРТ головного мозга, но не обучение данному процессу.
Как выглядит снимок МРТ головного мозга
Классический пример МРТ снимков головного мозга показан на рисунках ниже. Магнитно-резонансная томография выполняется в поперечной (или аксиальной – рисунок снизу) и продольной (или сагиттальной — рисунок сверху) плоскостях.
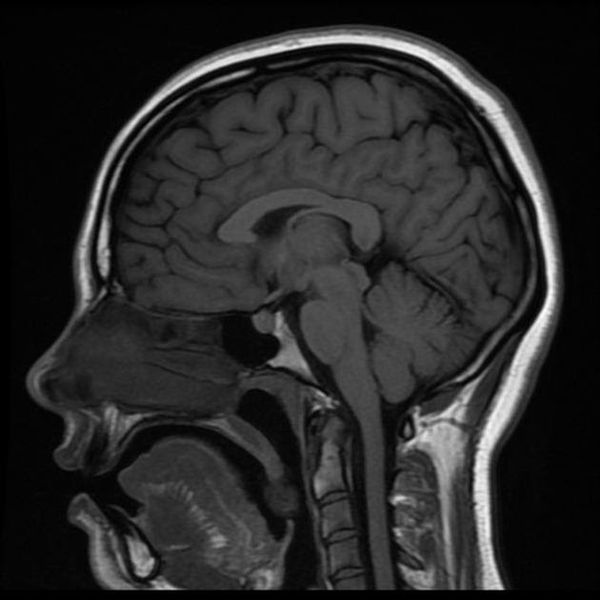
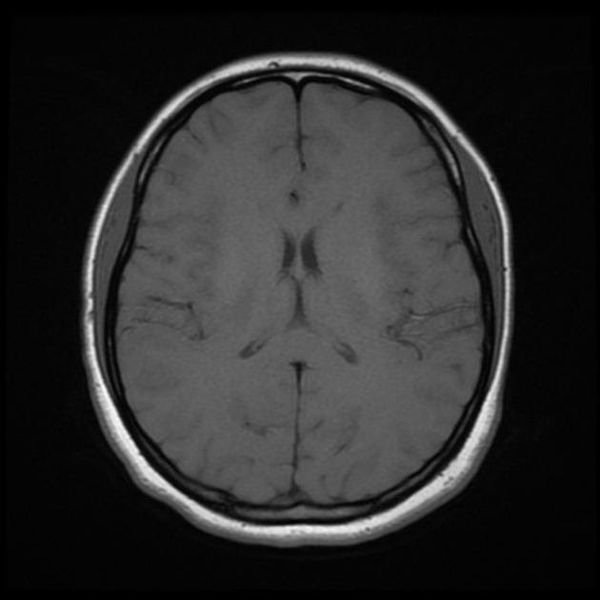
Исследование выполняется в нескольких режимах. Основные из них Т1 и Т2. Изображения, полученные в данных режимах, часто также называют Т1-взвешенными или Т2-взвешенными снимками. Изображения, показанные выше, сделаны в Т1-режиме.
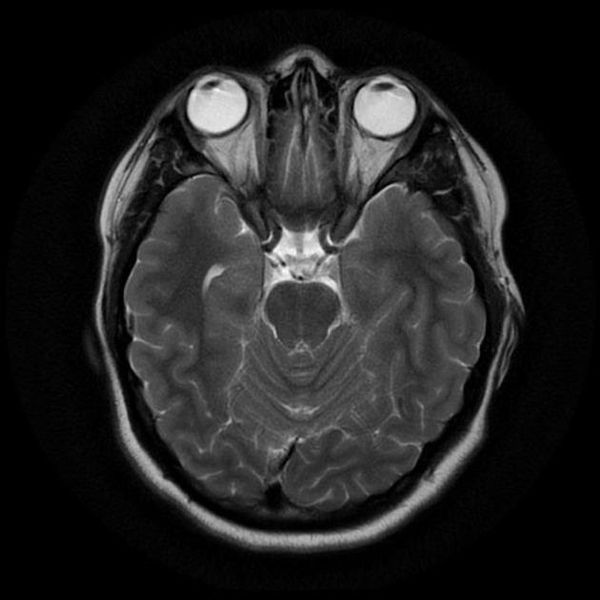
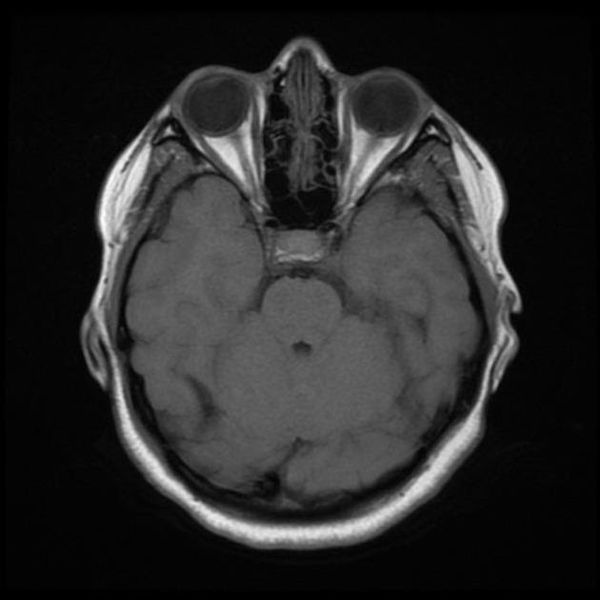
Главное отличие этих режимов – в том, как на снимках отображается жидкость и воздух. В Т1 режиме ткани, содержащие большое количество воды, имеют более темную окраску, в то время как в Т2 режиме они яркие, светлые. Это легко понять, посмотрев на снимки выше – глазные яблоки визуализируются в виде светлых парных округлых образований с одной стороны яркие и светлые, с другой – темные. Следовательно, снимок справа сделан в Т1 режиме, снимок слева – в Т2. Также существует разница в том, как в этих режимах отображается серое вещество головного мозга. В Т2 режиме оно светлее, чем белое вещество.
На самом деле режимов намного больше – FLAIR, DWI, STIR и так далее. Какой-то режим используется для подавления сигнала от богатых жиром тканей, какой-то – для изучения плотности распределения протонов в тканях, третий – для оценки броуновского движения молекул воды. Вот почему полный курс МРТ-диагностики для врачей длится не один месяц.
Норма и отклонения на МРТ головного мозга
Как же узнать, есть ли на снимках признаки болезни? Самое главное – запомнить, как выглядит головной мозг здорового человека. Врач, изучая снимки пациентов, постоянно сравнивает их с нормальными снимками, хранящимися у него в голове. Чтобы понять, как это происходит – посмотрите на снимки внизу:
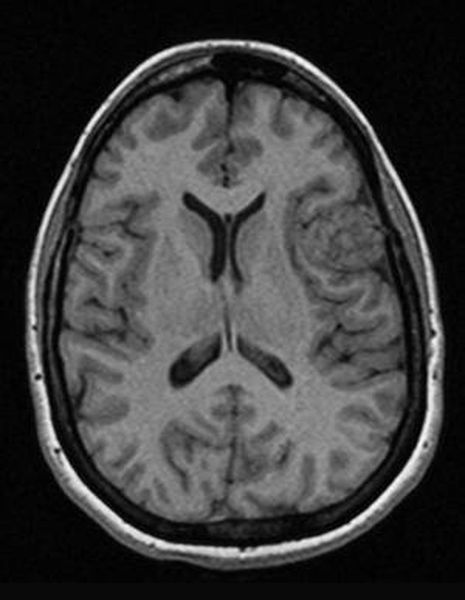
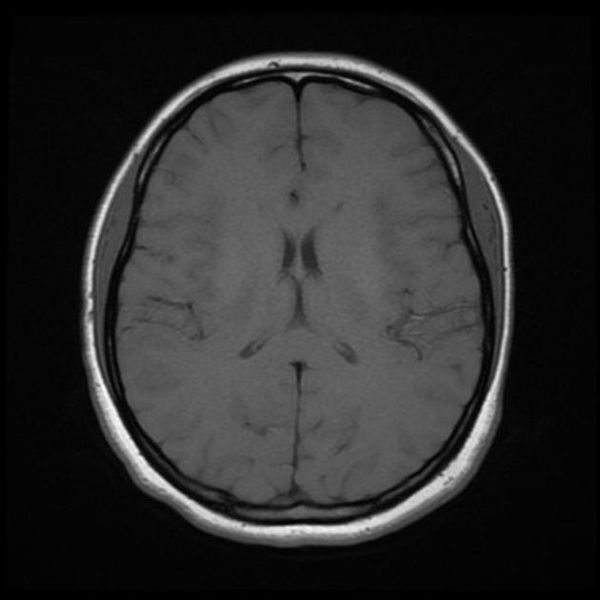
Перед вами – два снимка, сделанных в одном режиме. Снимок снизу – норма. Какое заболевание, в таком случае, есть на верхнем снимке? Чтобы понять это, нужно сравнить эти изображения. Явно видно отличие – на верхнем снимке в правой части головного мозга есть новообразование. Разница еще заметнее, если сравнить левую и правую части того же снимка.
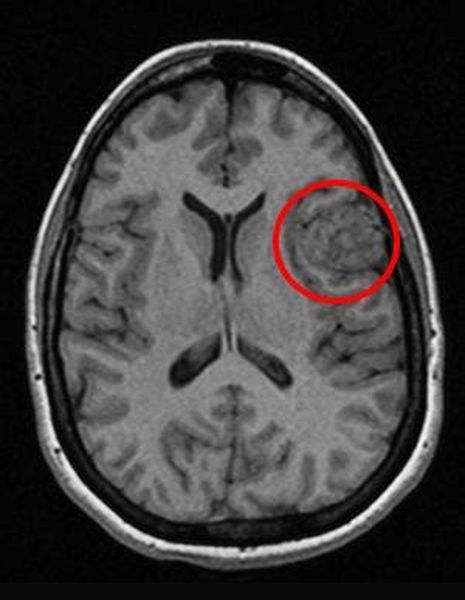
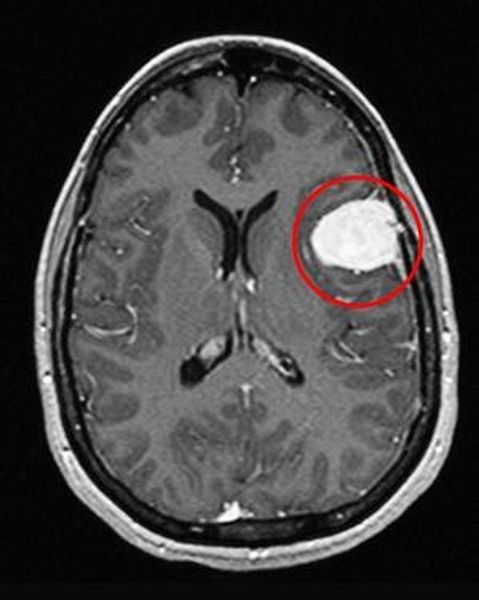
Отметим его красной окружностью. Визуально оно представляет собой узел, неоднородный по окраске и отличающийся от серого и белого вещества головного мозга. В таких случаях, чтобы точно определить границы опухоли и определить её тип исследование повторяют с контрастом. Введение контрастного препарата в кровь через локтевую вену приводит к накоплению контрастного вещества в тканях опухоли – нормальные здоровые ткани его практически не накапливают. И мы получаем следующую картину, показанную на рисунке справа. Яркая окраска опухоли соответствует накопленному контрасту – теперь можно не только сказать, где опухоль, но и примерно определить, что это доброкачественная опухоль, так как она имеет четкие границы (злокачественные опухоли прорастают окружающие ткани, из-за чего границы будут размытыми и не такими четкими).
Таким образом расшифровка результатов МРТ головного мозга проводится путем сравнения полученных снимков с нормой. При отсутствии отличий можно говорить о том, что пациент, чьи снимки исследует врач, скорее всего здоров. Сравнивается все – форма, размеры анатомических структур, локализация, симметричность, количество спинномозговой жидкости в полостях головного мозга, и множество других параметров. Каждое заболевание, будь то инсульт или рассеянный склероз, имеет свои характерные признаки.
Как читать результаты МРТ головного мозга
Теперь попробуем прочитать заключение МРТ головного мозга с расшифровкой снимков на следующем примере:

- Техника сканирования – перечисляются режимы, в которых проводилось исследование;
- На серии томограмм определяются мелкие очаги ишемии – участки белого вещества головного мозга, испытывающие дефицит кислорода (возрастные изменения). Любые очаговые изменения вне зависимости от локализации — патология;
- Далее описывается кора головного мозга – незначительная атрофия лобно-височных долей также является возрастными изменениями (исследование проводилось у пожилого человека);
- Затем описывается система желудочков головного мозга – полостей, в которых циркулирует спинномозговая жидкость – если они не расширены, имеют нормальную форму, значит все в норме.
- Мозолистое тело, мозжечок и ствол мозга без изменений;
- Далее идет описание гипофиза – железы, расположенной на основании мозга (незначительное уплощение возможно в норме), области перекреста зрительных нервов, синусы внутренней сонной артерии – также без изменений, так как нет асимметрии, их контуры четкие и ровные;
- Затем идет описание глазных яблок и содержимого глазниц – без патологических сигналов, т.е. в норме;
- Область мостомозжечкового угла – место отхождения слухового или преддверно-улиткового нерва, отвечающего за слух – без изменений, нерв определяется с обеих сторон;
- Описываются придаточные пазухи носа – в правой гайморовой пазухе имеется киста – остальные пазухи в норме, пневматизация обычная (содержат воздух, а не гной или жидкость);
- Далее идет исследование сосудов головного мозга или МР-ангиография – отсутствие изменений калибра, симметричность, отсутствие смещения и сужения просвета – норма. Небольшое сужение допускается;
- Затем проводится венография – отсутствие изменений и нормальный калибр – норма.
В заключение выносят только патологические изменения – в данном случае это очаги ишемии, атрофия лобно-височных областей, киста гайморовой пазухи. В целом картина соответствует возрасту пациента – 65 лет. МРТ-признаки сосудистой энцефалопатии – окончательный диагноз будет определен лечащим врачом. Обратите внимание – в норме на снимках отсутствуют изменения, очаговые или диффузные (распространенные равномерно), кисты, опухоли, новообразования, участки патологической гипер или гипоинтенсивности сигнала. Анатомические образования имеют четкие ровные контуры, не смещены, симметричны. Сосуды симметричны, без признаков сужения просвета, с нормальным ходом и калибром, интралюминарный сигнал (фактически кровь в сосуде) гомогенный, что говорит об отсутствии тромбов в просвете артерии или вены.
Подобным путем проводится расшифровка и описание снимков в любой клинике. Однако точность сделанного заключения зависит от квалификации врача МРТ-диагностики.
ТТГ щитовидной железы
ТТГ, тиреотропный гормон, вырабатываемый гипофизом. ТТГ стимулирует выработку гормонов щитовидки. Именно эти вещества отвечают за обмен жиров, белков и углеводов в организме, а также за работу сердечно-сосудистой, половой систем, влияют на психоэмоциональное состояние человека и действие ЖКТ. Эндокринологи, как правило, проверяют уровень ТТГ вместе с гормонами щитовидки.
Анализ на уровень ТТГ

Контроль уровня тиреотропного гормона в крови обязателен для пациентов, страдающих от любых, даже незначительных патологий щитовидной железы. По мнению американских эндокринологов, анализ на ТТГ также ежегодно необходимо сдавать женщинам старше 50 лет.
За два дня до проведения анализа пациенту следует исключить курение и физические нагрузки. Кровь на ТТГ берут утром, натощак. Если эндокринолог хочет отследить изменение уровня гормона, анализ проводится в одно и то же время суток.

Норма ТТГ
Определить нормальный для пациента уровень ТТГ под силу только лечащему эндокринологу. Нормативные показатели гормона отличаются в зависимости от пола, возраста пациента и даже времени суток. Например, утром наблюдается наибольшая концентрация гормона в крови, а у многих беременных женщин фиксируется низкий ТТГ.
Высокий ТТГ
Повышенный ТТГ может быть признаком таких заболеваний, как:
- гипотиреоз
- воспаления щитовидной железы;
- первичная надпочечниковая недостаточность.
Однако повышенный уровень ТТГ не всегда является сигналом о заболевании. Показатель увеличивается вследствие физической нагрузки, ввиду приема ряда медицинских препаратов, например, нейролептиков, йодидов, бета-адреноблокаторов, преднизолона и других медицинских препаратов. ТТГ выше нормы нередко фиксируется после гемодиализа, удаления желчного пузыря. У беременных также очень часто наблюдается повышенный уровень ТТГ.
Высокий ТТГ: симптомы
Высокий уровень тиреотропного гормона (ТТГ) проявляется в таких симптомах, как:
- утолщение шеи;
- слабость;
- отечность, бледность кожи;
- раздражительность, нарушение сна;
- плохой аппетит;
- тошнота;
- запоры;
- понижение температуры тела;
- невнимательность, заторможенность, замедленное мышление, апатия, депрессия.
Низкий ТТГ
Пониженный уровень ТТГ указывает на такие заболевания, как:
- болезнь Пламера;
- стресс;
- острое воспаление щитовидной железы;
- токсический зоб.
Низкий ТТГ нередко связан с передозировкой гормональных препаратов. Снижение уровня гормона также может спровоцировать голодание или сильный стресс.
Низкий ТТГ: симптомы
Основными симптомами низкого уровня тиреотропного гормона являются:
- повышение температуры;
- тахикардия, учащенное сердцебиение;
- повышенное давление;
- головные боли;
- повышенный аппетит;
- расстройства желудка;
- эмоциональная неуравновешенность.

ТТГ при беременности
При беременности норма ТТГ составляет около 0,2¬-3,5 мЕд/л. Эндокринологи рекомендуют регулярно сдавать анализы у эндокринолога в течение всего срока беременности, обычно ТТГ понижен в первом триместре.
При многоплодной беременности низкий показатель ТТГ наблюдается у 100% женщин, при одноплодной — у 20-30% подавляется выработка гормона.
Норму ТТГ для женщины при беременности определяет лечащий врач. При необходимости пациентке назначают дополнительные обследования:
- тонкоигольную аспирационную биопсию щитовидки (ТАБ);
- эхографическое обследование.
При высоком ТТГ женщине назначают терапию L-тироксином (L-T4).
Антитела к рецепторам ТТГ
Как мы уже говорили, именно рецепторы ТТГ регулируют синтез гормонов в щитовидной железе. При нарушении работы иммунной системы, вырабатываются антитела к рецепторам тиреотропного гормона.
Выделяют три типа антител:
- Блокаторы рецепторов ТТГ — снижают уровень гормонов ТЗ и Т4;
- Связующие с рецептором — эти сильные антитела провоцируют долгосрочное повышение уровня гормонов Т3 и Т4;

ТТГ: лечение
Если вы подозреваете у себя низкий или высокий уровень ТТГ, ни в коем случае не стоит заниматься самолечением. Определить, повышен или понижен у больного ТТГ может только опытный врач на основании анализов и осмотра.
Высокий ТТГ: лечение
Если в результате анализов было обнаружено, что тиреотропный гормон выше нормы и варьирует в диапазоне от 7,1 до 75 мкМЕ/мл, возможно, больной страдает от гипотиреоза. Врач назначает синтетический гормон щитовидной железы — тиротоксин.
Низкий ТТГ: лечение
Пониженный уровень тиреотропного гормона (до 0,01 мкМЕ/мл) требует комплексного обследования сердечно-сосудистой системы. Эндокринолог также проверяет уровни Т3 и Т4, чтобы исключить болезнь Грейвса и узловой зоб.
Куда обратиться?
При лечении эндокринной системы ключевым фактором успеха является выбор специалиста. Если вы подозреваете, что уровень ТТГ гормона отклоняется от нормы, не уверены в диагнозе, поставленном вашим врачом, хотите обследовать щитовидную железу, вас ждет Виктор Алексеевич Макарьин.
Виктор Алексеевич специализируется на операциях на щитовидной железе, паращитовидных железах, надпочечниках, является кандидатом медицинских наук и членом европейской ассоциации эндокринных хирургов. Виктор Алексеевич работает в одном из старейших многопрофильных стационаров Северной столицы, Университетская клиника.
Вы можете получить очную консультацию врача или связаться с Виктором Алексеевичем по скайпу. Звоните и записывайтесь на прием: +7 812 4083234
Определение стадии рака по системе TNM


- Стадия опухоли по системе TNM
- Общая стадия опухоли
Стадирование опухоли основано на трех критериях: глубина врастания опухоли в стенку кишки (Т), наличие распространения опухолевых клеток по лимфатическим узлам (N) и, наконец, наличие или отсутствие метастазов (M). Эти три составляющих образуют систему TNM для стадирования колоректального рака (см. таблицы ниже).
Стадия Т (tumor) – глубина врастания опухоли в стенку кишки. Чем меньше значение это стадии, тем менее инвазивный рост опухоли. Опухоль стадии Т0 можно еще считать достаточно доброкачественной, так как рост этой опухоли ограничен только слизистой оболочкой кишки. Опухоль стадии Т4 обозначает то, что опухоль проросла не только все слои кишечной стенки, но и соседние с ней органы.
Стадия N (lymphnodes) – обозначает количество лимфатических узлов, в которых были обнаружены раковые клетки. Стадия N0 обозначает, что при патологоанатомическом исследовании ни в одном из лимфатических узлов не были обнаружены клетки рака. Стадия Nx обозначает, что количество пораженных лимфатических узлов неизвестно. Это может быть на стадии обследования до операции, когда невозможно определить поражены лимфатические узлы или нет. Пока не проведено патологоанатомическое исследование, стадия считается как Nx.
Стадия М (metastases) – обозначает, имеются ли у опухоли отдаленные отсевы – метастазы.
Стадия опухоли по системе TNM
| T | N | M |
| is – рост опухоли в пределах слизистой | 0 – нет данных за поражение лимфатических узлов | 0 – нет данных за наличие отдаленных метастазов |
| 1 |
опухоль врастает, но не прорастает подслизистый слой кишки
поражение от 1 до 3 лимфатических узлов
наличие отдаленных метастазов опухоли
опухоль врастает, но не прорастает мышечный слой кишки
поражение больше, чем 3 лимфатических узлов
неизвестно, имеются ли метастазы
опухоль прорастает через мышечный слой в окружающие ткани
неизвестно, поражены ли лимфатические узлы
опухоль врастает в окружающие органы
Общая стадия опухоли
| T | N | M | |
|---|---|---|---|
| Стадия | 1,2 | 0 | 0 |
| Стадия | 3,4 | 0 | 0 |
| Стадия | Любая | 1,2 | 0 |
| Стадия | Любая | Любая | 1 |
Чтобы понять, как устанавливается стадия, найдите в таблице заголовки T, Nи M. В каждом столбце имеются цифры или слово «любая». Вторая строка в таблице соответствует стадии I, в столбцах имеются следующие данные: стадия Т 1 или 2, стадии Nи M – 0. Это означает, что если опухоль врастает только в стенку кишки (стадия Т1 или Т2) и ни в одном лимфоузле нет раковых клеток (стадия N0), и нет отдаленных метастазов (стадия M0), то опухоль будет классифицироваться, как рак I стадии. Опухоль, которая прорастает через кишечную стенку (стадия Т3 или T4), но при этом нет пораженных лимфатических узлов и отдаленных метастазов, имеет стадию II, и так далее.
Стадирование играет очень важную роль для определения тактики лечения. Для лечения опухолей I стадии обычно достаточно только хирургической операции, а опухоли III стадии обычно лечат, применяя и операцию, и химиотерапию. Таким образом, стадирование опухоли – это очень важный этап предоперационной диагностики. Для того, чтобы определить стадию до операции, может потребоваться выполнение многих исследований. Компьютерная томография (КТ), рентген грудной клетки, ультразвуковое исследование (УЗИ), магнитно-резонансная томография (МРТ) и позитронно-эмиссионная томография (ПЭТ) являются очень информативными исследованиями, помогающими определить степень распространения опухоли. Тем не менее, самым точным методом определения стадии опухоли является исследование удаленной во время операции части кишки с помощью микроскопа.
Очень важно, чтобы пациенты понимали принципы определения стадии опухоли, и имели представление о том, как это делается, чтобы грамотно обсуждать варианты и прогноз лечения с врачом.
